Soru 1 |
1 mol C2H6O2 bileşiği, 2 mol C atomu, 6 mol H atomu ve 2 mol O atomu olmak üzere toplam 10 mol atom içerir.
Verilen bilgiye göre aşağıdaki ifadelerden hangisi yanlıştır?
Toplam 2 mol atom içeren CH4 bileşiği 0,4 moldür. | |
1,5 mol H2O bileşiği 3 mol H atomu içerir. | |
2,5 mol CO2 bileşiği 5 mol C atomu içerir. | |
0,2 mol N2O3 bileşiği toplam 1 mol atom içerir. | |
0,4 mol O atomu içeren SO2 bileşiği 0,2 moldür. |
Soru 2 |
0,25 mol CO2 gazı ile ilgili bazı bilgiler şöyledir:
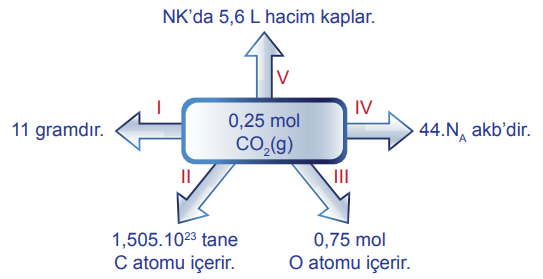
Buna göre verilen bilgilerden hangileri yanlıştır?
(C:12 g/mol, O:16 g/mol, NA:Avogadro sayısı = 6,02.1023)
Yalnız II. | |
I ve II. | |
I ve IV. | |
III ve IV. | |
III ve V. |
Soru 3 |
Normal koşullarda (1 atm basınç, 0°C sıcaklık) bir mol gaz 22,4 litre hacim kaplar.
Buna göre,
I. 1 mol atom içeren O2 gazı,
II. 44 gram CO2 gazı,
III. 4.NA tane hidrojen atomu içeren CH4 gazı
maddelerinden hangilerinin normal koşullarda hacmi 22,4 litredir?
(C:12 g/mol, O:16 g/mol, NA:Avogadro sayısı)
Yalnız I. | |
Yalnız III. | |
I ve II. | |
II ve III. | |
I, II ve III. |
Soru 4 |
1 mol C3H6 bileşiğinde 6,02.1023 tane molekül vardır.
Buna göre 1,806.1022 tane molekül içeren C3H6 bileşiği ile ilgili verilen bilgilerden hangisi yanlıştır?
(H:1 g/mol, C:12 g/mol)
3.10-2 moldür. | |
9.10-2 mol C atomu içerir. | |
2.10-2 gram H atomu içerir. | |
0,27 mol atom içerir. | |
1,26 gramdır. |
Soru 5 |
Kimyasal tepkimelerde tepkimeye giren maddelerin atom tür ve sayısı ürünlerinkine eşittir. Eşit değilse tepkimenin uygun katsayılarla denkleştirilmesi gerekir.
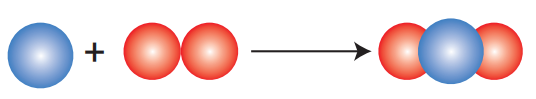
Bu bilgiye göre aşağıdaki tepkimelerden hangisinin denkleştirilmesi gerekir?
2H2 + O2 → 2H2O | |
C2H5OH + 3O2 → 2CO2 + 3H2O | |
2NH3 + CO2 → CO(NH2)2 + H2O | |
CS2 + O2 → CO2 + 2SO3 | |
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O |
Soru 6 |
Kimya öğretmeni 66,2 gram Pb(NO3)2 katısını 100 mL suda çözerek 1. çözeltiyi, 33,2 gram KI katısını 100 mL suda çözerek 2. çözeltiyi hazırlıyor. Daha sonra 1. ve 2. çözeltileri farklı bir kapta karıştırarak bir katı çökeleğin oluştuğunu öğrencilerine gösteriyor. Aynı zamanda tahtaya
Pb(NO3)2(suda) + 2KI(suda) → PbI2(k) + 2KNO3(suda)
tepkimesini yazarak, karıştırma sırasında bu tepkimenin gerçekleştiğini söylüyor ve çöken katının kaç gram olduğunu öğrencilerine soruyor.
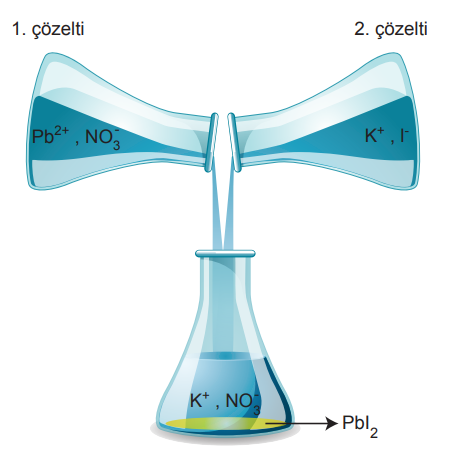
Buna göre öğrencilerin verdiği doğru cevap aşağıdakilerden hangisidir?
(KI:166 g/mol, Pb(NO3)2:331 g/mol, PbI2:461 g/mol)
16,6 | |
23,5 | |
33,2 | |
33,1 | |
46,1 |
Soru 7 |
CO(g) + ![]() O2(g) → CO2(g) tepkimesinde 1 mol CO ile 0,5 mol O2 tepkimeye girmektedir. Tepkimeye girenler 1’er mol alınırsa 0,5 mol O2 artar.
O2(g) → CO2(g) tepkimesinde 1 mol CO ile 0,5 mol O2 tepkimeye girmektedir. Tepkimeye girenler 1’er mol alınırsa 0,5 mol O2 artar.
Buna göre,
2Ag(k) + O2(g) → 2AgO(k)
tepkimesine girenler 2’şer mol alınırsa hangi maddeden kaç mol artar?
1 mol O2 | |
0,5 mol Ag | |
0,5 mol O2 | |
0,25 mol Ag | |
1,25 mol Ag |
Soru 8 |
Bir kimyasal tepkimede tamamen tükenen maddeye sınırlayıcı bileşen denir. Sınırlayıcı bileşene göre oluşan ürünlerin miktarı belirlenir.
Krom elementinin 1,04 gramı ile oksijen gazının 0,64 gramı tepkimeye girerek tam verimle Cr2O3 katısı oluşuyor.
Buna göre tepkime ile ilgili,
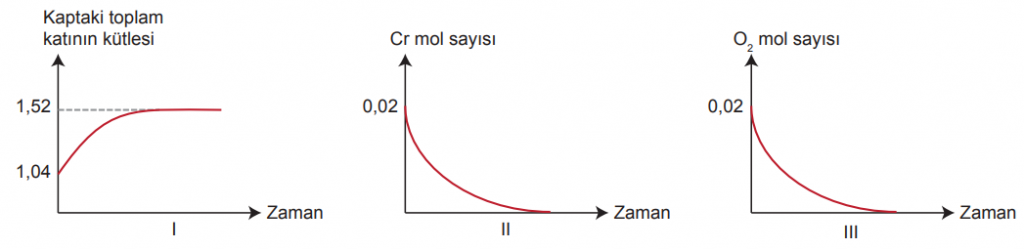
grafiklerinden hangileri doğrudur?
(O:16 g/mol, Cr:52 g/mol)
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 9 |
Saf olmayan madde kullanılan tepkimelerde elde edilecek ürünün miktarı bulunurken saflık yüzdesinin de dikkate alınması gerekir.
Buna göre %80 saflıkta CaCO3 içeren 50 gramlık bir karışım,
CaCO3(k) → CaO(k) + CO2(g)
tepkimesine göre ayrıştığında NK’da en fazla kaç litre CO2 gazı elde edilir?
(C:12 g/mol, O:16 g/mol, Ca:40 g/mol)
5,6 | |
6,72 | |
8,96 | |
11,2 | |
13,44 |
Soru 10 |
Kimyasal hesaplamalar teorik sonuçlar üzerinden yapılır. Ancak deneylerde elde edilen sonuçlar her zaman teorik sonuçlar ile örtüşmez. Bu durumda %verim = ![]() 100 formülü kullanılarak yüzde verim hesaplaması yapılır.
100 formülü kullanılarak yüzde verim hesaplaması yapılır.
Neşe, Mg(k) + 2HCl(suda) → MgCl2(suda) + H2(g) tepkimesini gerçekleştirecek bir deney tasarlıyor.
1 mol Mg ve 2 mol HCl alarak gerçekleştirdiği tepkimeden 47 g MgCl2 oluştuğunu gözlemliyor.
Teorik olarak hesapladığı sonucu ile deneysel sonucu örtüşmeyen Neşe, bu deneyde yüzde kaç verim elde etmiştir?
(H:1 g/mol, Mg:24 g/mol, Cl:35 g/mol)
100 | |
75 | |
50 | |
25 | |
12,5 |
10. Sınıf Kimya Kimyanın Temel Kanunları ve Kimyasal Hesaplamalar PDF Test
10. Sınıf Kimya Kimyanın Temel Kanunları ve Kimyasal Hesaplamalar konusuyla ilgili sorular bulunmaktadır. Testler; kazanım odaklı güncel sorulardan oluşmaktadır.
Test İstatistikleri (Ortalama)
| Doğru | 4.25 |
| Yanlış | 3.25 |
| Net | 3.17 |
| Çözülme Sayısı | 4 |
Başarı Tablosu
| İsim Soyisim | Doğru | Yanlış | Süre |