Soru 1 |
Aşağıdaki şekilde H2 ile I2 molekülleri arasındaki kimyasal tepkime gösterilmiştir.
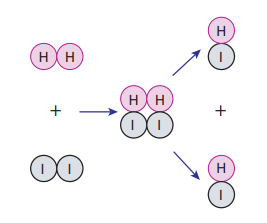
Buna göre,
I. H2 ve I2 molekülleri etkin çarpışma yapmıştır.
II. H2I2 molekülü HI molekülünden daha kararlıdır.
III. H2I2 molekülü aktifleşmiş komplekstir.
yargılarından hangileri doğrudur?
Yalnız I. | |
Yalnız II. | |
I ve II. | |
I ve III. | |
I, II ve III. |
Soru 2 |
Çarpışma teorisine göre;
□ Ürün oluşumu ile sonuçlanan çarpışmalara etkin çarpışma denir.
□Birim zamanda oluşan etkin çarpışma sayısı ile tepkime hızı doğru orantılıdır.
□Her çarpışma tepkime ile sonuçlanır.
□Tepkime olması için çarpışan taneciklerin yeterli kinetik enerjiye sahip olması gerekir.
Verilen cümlelerden doğru (D), yanlış (Y) ile sırasıyla işaretlenirse aşağıdakilerden hangisine ulaşılır?
Soru 3 |
2XY(g) → X2(g) + Y2(g)
tepkimesine ait potansiyel enerji-tepkime koordinatı grafiği aşağıda verilmiştir.
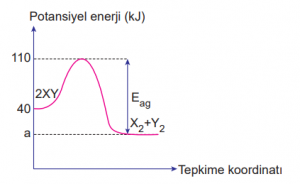
Tepkimenin ∆H değeri -30 kJ olduğuna göre, ürünlerin potansiyel enerjisi (a) ve geri aktifleşme enerjisi (Eag) aşağıdaki seçeneklerin hangisinde doğru verilmiştir?
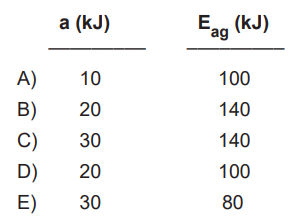
A | |
B | |
C | |
D | |
E |
Soru 4 |

Verilen tepkimelerin hızlarını ölçmek için uygun gözlemsel niceliklerle eşleştirilmesi aşağıdakilerden hangisidir?
I-a II-b III-c | |
I-b II-a III-c | |
I-c II-b III-a | |
I-a II-c III-b | |
I-b II-c III-a |
Soru 5 |
N2(g) + 3H2(g) → 2NH3(g)
tepkimesine göre 2 litrelik kapalı bir kapta 40 saniyede 1,6 mol N2 gazı harcanmaktadır.
Buna göre NH3 gazının oluşma hızı kaç mol/L.s'dir?
2.10-2 | |
4.10-2 | |
6.10-2 | |
8.10-2 | |
9.10-2 |
Soru 6 |
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(g)
tepkimesinde yer alan maddelerin hızları arasındaki ilişki aşağıdakilerden hangisidir?
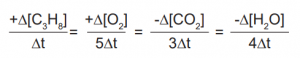 | |
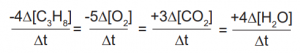 | |
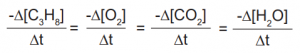 | |
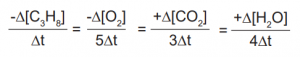 |
Soru 7 |
aX(g) + bY(g) → cZ(g)
Yukarıdaki tepkimeyle ilgili aşağıdaki bilgiler veriliyor.
– X gazının ortalama harcanma hızı Y gazının ortalama harcanma hızının 3 katıdır.
– Z gazının ortalama oluşum hızı X gazının ortalama harcanma hızının ![]() katıdır.
katıdır.
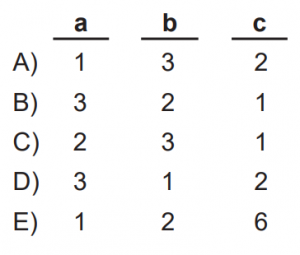
Buna göre a, b ve c değerleri seçeneklerden hangisi gibi olabilir?
A | |
B | |
C | |
D | |
E |
Soru 8 |
Bir kimyasal tepkimede ürün oluşabilmesi için,
I. tepkimeye girenlerin yeterli enerjiye ve hıza sahip olması,
II. tepkimeye girenlerin etkin çarpışması,
III. reaktiflerin aynı fiziksel hâlde olması
koşullarından hangileri gereklidir?
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 9 |
2N2O5(g) → 4NO2(g) + O2(g)
tepkimesine göre N2O5 gazının derişimi 5 dakikada 1,5 mol/L’den 0,3 mol/L’ye azaldığına göre, O2 gazının ortalama oluşma hızı kaç mol/L.s’dir?
4.10-3 | |
3.10-3 | |
2.10-3 | |
1.10-3 | |
1.10-4 |
Soru 10 |
CH4(g) + 2O2(g)→ CO2(g) + 2HO2(g)
tepkimesine göre 4,8 gram CH4 gazının tamamı 2 dakikada yanmaktadır.
Buna göre, CO2 gazının ortalama oluşma hızı kaç mol/s’dir? (C:12 g/mol, H:1 g/mol)
2,5.10-6 | |
2,5.10-5 | |
2,5.10-4 | |
2,5.10-3 | |
1,25.10-3 |
Soru 11 |
Aşağıda bazı tepkimeler verilmiştir.
I. 2H2(g) + O2(g) → 2H2O(s)
II. C(k) + 2H2(g) → CH4(g)
III. 2NO(g) + O2(g) → 2NO2(g)
Buna göre hangileri heterojen faz tepkimelerine örnektir?
Yalnız I. | |
Yalnız III. | |
I ve II. | |
II ve III. | |
I, II ve III. |
11. Sınıf Kimya Kimyasal Tepkimelerde Hız PDF Test
11. Sınıf Kimya Kimyasal Tepkimelerde Hız konusuyla ilgili sorular bulunmaktadır. Testler; kazanım odaklı güncel sorulardan oluşmaktadır.
Test İstatistikleri (Ortalama)
| Doğru | 6 |
| Yanlış | 2 |
| Net | 5.33 |
| Çözülme Sayısı | 1 |
Başarı Tablosu
| İsim Soyisim | Doğru | Yanlış | Süre |