Soru 1 |
0,5 mol CS2 bileşiğinin yeterli O2 ile yakılmasından CO2 ve SO2 gazları oluşuyor ve 300 kj ısı açığa çıkıyor
Buna göre;
I. CS2’nin molar yanma ısısı 600 kj’dür.
II. CS2’nin standart oluşum entalpisi -410 kj/ mol’dür.
III. Oluşan CO2 sıvı olsaydı açığa çıkan enerji artardı.
Yargılarından hangileri doğrudur?
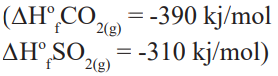
Yalnız I | |
Yalnız II | |
Yalnız III | |
I ve II | |
II ve III |
Soru 2 |
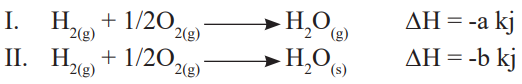
Yukarıda verilen tepkimeler ile ilgili;
I. H2O gazı oluşurken açığa çıkan enerji daha fazladır.
II. Her iki tepkimede molar oluşum tepkimesidir.
III. Oluşan bileşiğin fiziksel hali tepkime entalpisini değiştirir.
Yargılarından hangileri doğrudur?
Yalnız I | |
Yalnız II | |
I ve II | |
II ve III | |
I, II ve III |
Soru 3 |
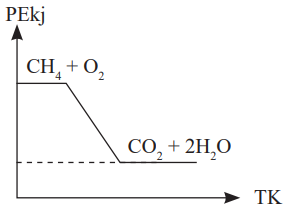
1 mol CH4 gazının yakılmasına ait PE - TK grafiği yukarıdaki gibidir. Buna göre;
I. CH4 gazının yanması ekzotermiktir.
II. Tepkime başladıktan sonra kendiliğinden devam eder.
III. Tepkimedeki entalpi değişimi ∆H=800 kj’dür.
Yargılarından hangileri doğrudur?
![]()
Yalnız I | |
Yalnız II | |
Yalnız III | |
I ve II | |
I, II ve III |
Soru 4 |
6 gram C2H6 gazının yakılmasından açığa çıkan ısıyı hesaplayabilmek için;
I. CO2 ve H2O’nun molar oluşum ısıları
II. C2H6 gazının molar yanma ısısı
III. C2H6 gazının molar oluşum ısısı
Hangilerinin tek başına bilinmesi yeterlidir?
(C:12 H:1)
Yalnız I | |
Yalnız II | |
Yalnız III | |
I ve II | |
II ve III |
Soru 5 |
CH4 ve C2H6 gazlarının molar yanma ısıları sırasıyla -800 kj ve -1400 kj’dür. Molce %90 oranında
CH4 gazından oluşan bir miktar doğalgaz (CH4+C2H6) yakıldığında 1720 kj ısı açığa çıkıyor.
Buna göre karışım kaç moldür?
0,2 | |
0,5 | |
1 | |
2 | |
4 |
Soru 6 |
H2S bileşiğinin standart molar oluşum entalpisi ekzotermiktir.
Buna göre H2S(g), H2S(s) ve H2S(k) bileşiklerinden standart koşullarda 1’er mol oluşumu sırasında açığa çıkan ısıların karşılaştırılması hangi seçenekte doğru verilmiştir?
H2S(s) = H2S(g) = H2S(k) | |
H2S(g) > H2S(s) > H2S(k) | |
H2S(k) > H2S(s) > H2S(g) | |
H2S(g) > H2S(s) = H2S(k) | |
H2S(s) > H2S(k) > H2S(g) |
Soru 7 |
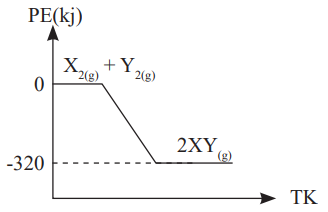
Yukarıda verilen PE - TK grafiğine göre;
I. Tepkime ısı verendir.
II. Tepkimedeki entalpi değişimi -320 kj’dür.
III. XY gazının molar oluşum entalpisi 160 kj’dür.
Yargılarından hangileri doğrudur?
Yalnız I | |
I ve II | |
I ve III | |
II ve III | |
I, II ve III |
Soru 8 |
![]()
Yukarıda verilen tepkimeler ve entalpi değişimlerine göre CO gazının molar yanma ısısı
nedir?
280 | |
500 | |
-280 | |
-500 | |
-400 |
Soru 9 |
![]()
Yukarıda verilen tepkimeler ile ilgili;
I. ∆H1 ve ∆H2 sırasıyla SO2 ve SO3 gazlarının molar oluşum ısılarıdır.
II. 12,8 gram SO2 gazı oluşurken 58 kj ısı açığa çıkar.
III. Eşit kütlede SO2 ve SO3 gazı oluşturulursa 1. tepkimede daha fazla ısı açığa çıkar.
Yargılardan hangileri doğrudur?
(SO2: 64 SO3: 80)
Yalnız I | |
Yalnız II | |
Yalnız III | |
I ve II | |
II ve III |
Soru 10 |
“8 gram C3H4 gazının yakılması ile 240 kj ısı açığa çıkmaktadır.”
Bu bilgiye göre;
I. C3H4 gazının molar yanma ısısı
II. C3H4 gazının molar oluşum ısısı
III. C3H4 gazının molar yoğunlaşma ısısı
Hangileri hesaplanabilir?
(C:12 H:1)
Yalnız I | |
Yalnız II | |
I ve II | |
II ve III | |
I, II ve III |
11. Sınıf Kimya Oluşum Entalpisi PDF Test
11. Sınıf Kimya Oluşum Entalpisi konusuyla ilgili sorular bulunmaktadır. Testler; kazanım odaklı güncel sorulardan oluşmaktadır.
Test İstatistikleri (Ortalama)
Başarı Tablosu
| İsim Soyisim | Doğru | Yanlış | Süre |