Soru 1 |
Laboratuvarda 0,1 M 100 mL NaCl çözeltisi hazırlamak için izlenecek yol ile ilgili bilgiler aşağıda karışık olarak verilmiştir.
I. Tartılan katı, balon jojeye konur.
II. n=M.V formülünden gerekli katı miktarının mol sayısı hesaplanır.
III. Balon jojeye konulan katının üzerine saf su ilave edilerek, hacim 100mL’ye tamamlanır.
IV. Hesaplanan katı miktarı hassas terazide ölçülür.
V. m=n.MA formülünden gerekli katı kütlesi hesaplanır.
Buna göre, çözelti hazırlanırken yukarıdaki işlemler hangi sıra ile yapılmalıdır?
II - V - IV - I - III | |
II - III - IV - I - V | |
I - III - IV - II - V | |
I - IV - III - V - I | |
III - I - II - IV - V |
Soru 2 |
Aşağıdaki çözeltide tanecikler arasında bulunan etkileşim türleri;
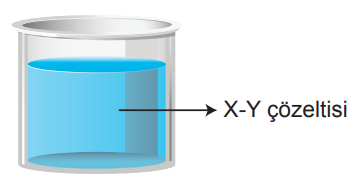
• İyon – dipol etkileşimi,
• Dipol – dipol etkileşimi,
• Hidrojen bağı
olduğuna göre,
I. X maddesi NH3, Y maddesi H2O olabilir.
II. X maddesi H2O, Y maddesi NaCl olabilir.
III. X maddesi HF, Y maddesi H2O olabilir.
ifadelerinden hangileri doğrudur?
(1H, 7N, 8O, 9F, 11Na, 17CI)
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 3 |
1 L çözeltide çözünmüş maddenin mol sayısına o çözeltinin molar derişimi denir.
500 mL 0,5 M NaCl sulu çözeltisi 200 mL ve 300 mL olacak şekilde 2 ayrı kaba konuluyor.

Buna göre,
I. 1. kaptaki çözeltinin derişimi daha azdır.
II. 2. kaptaki çözeltide, 1. kaptaki çözeltiye göre daha az miktarda çözünmüş NaCl bulunur.
III. 1. kaptaki çözelti derişimi 0,3 M, 2. kaptaki çözelti derişimi 0,2 M olur.
ifadelerinden hangileri doğrudur?
Yalnız I. | |
Yalnız II. | |
Yalnız III. | |
I ve II. | |
II ve III. |
Soru 4 |
200 mililitre 0,5 molar KCl sulu çözeltisi, 2 molar KCl çözeltisi kullanılarak hazırlanmak isteniyor.
Buna göre,
I. 100 mililitre saf suya 2 molar KCl çözeltisinden 100 mililitre eklenir.
II. 50 mililitre 2 molar KCl çözeltisinin hacmi saf su ile 200 mililitreye tamamlanır.
III. 20 mililitre 2 molar KCl çözeltisine 180 mililitre saf su eklenir.
işlemlerinden hangileri uygulanabilir?
(İşlemler sırasında toplam hacmin değişmeyeceği kabul edilecektir.)
Yalnız I. | |
Yalnız II. | |
Yalnız III. | |
I ve II. | |
II ve III. |
Soru 5 |

Kütlece yüzde derişimi 50’dir. | |
Molal derişimi | |
90 gram C6H12O6 çözünmüştür. | |
200 mL çözeltinin molar derişimi 2,5 mol/L’dir. | |
Suyun miktarı 180 gramdır. |
Soru 6 |
Aşağıda 1 atm dış basınçta 100 g saf suya 0,2 mol NaCl eklenerek elde edilen çözeltinin sıcaklık – zaman grafiği verilmiştir.
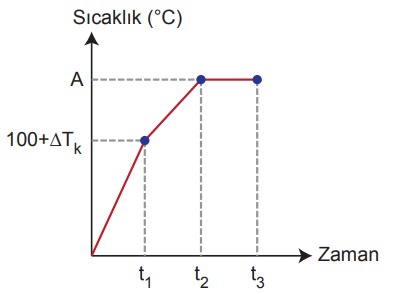
Grafiğe göre,

yargılarından hangileri doğrudur?
(Su için Kk = 0,52°C/m)
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 7 |
Bir çözeltinin kaynama ve donmaya başladığı sıcaklık, saf çözücüsünün kaynama ve donma sıcaklığından farklıdır.
Saf sıvıda katı bir madde çözünürse kaynama sıcaklığı artar. Bu artış çözeltinin molalitesi, çözünen madde iyonik ise formülündeki iyon sayısı ve çözücünün kaynama noktası artış sabiti ile doğru orantılıdır.
1 atm dış basınçta su ile hazırlanan 0,5 molal AlCl3 çözeltisinin kaynamaya başladığı sıcaklık 101,04°C’tur.
Buna göre 1 atm dış basınçta aşağıda verilen maddelerin suda çözünmesi ile hazırlanan çözeltilerden hangisinin kaynamaya başlama sıcaklığı yanlıştır?
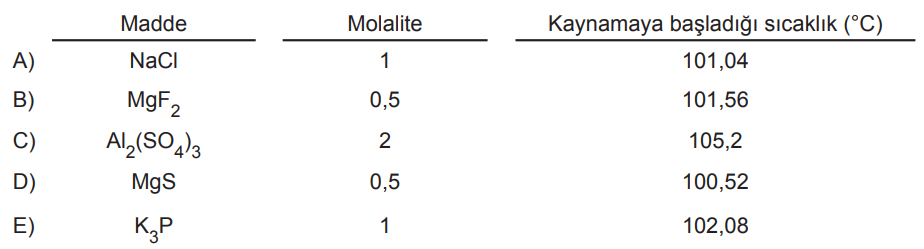
A | |
B | |
C | |
D |
Soru 8 |
Şekildeki derişik ve seyreltik tuzlu su çözeltileri yarı geçirgen bir zarla ayrılmıştır.
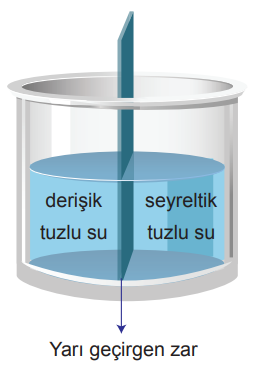
Suyun seyreltik ortamdan derişik ortama kendiliğinden geçişine osmoz denir.
Buna göre aşağıdakilerden hangisi osmoz olayı ile ilgilidir?
Denizde uzun süre kalan kişinin parmaklarının buruşması | |
Araba radyatörlerinin suyuna antifriz konulması | |
Soğuk havalarda uçakların kanatlarının alkolle yıkanması | |
Soğuk sularda daha fazla canlının yaşaması | |
Dalgıçların vurgun yememek için yüzeye dinlenerek çıkması |
Soru 9 |
Suya uçucu olmayan çözünen eklenerek hazırlanan çözeltilerin kaynamaya başlama sıcaklıkları, saf suyun kaynama noktasından yüksektir.
Sıvı çözeltilerde kaynama sıcaklığının değişme koşullarını araştıran bir öğrenci, aşağıdaki kaplara üzerlerinde belirtilen miktardaki maddeleri ilave ederek tamamen çözünmelerini sağlamıştır. Daha sonra oluşan çözeltileri çökelme olmadan ısıtıp kaynamaya başlama sıcaklıklarını ölçmüştür.

Çözeltilerin kaynamaya başlama sıcaklıklarının 1 > 2 > 3 şeklinde sıralandığını gözlemleyen öğrenci,
I. Sıvıda çözünen maddenin moleküler veya iyonlaşarak çözünmesi, çözeltinin kaynamaya başlama sıcaklığındaki artışı etkilemez.
II. Çözünen maddenin suya verdiği tanecik sayısı ile çözeltinin kaynamaya başlama sıcaklığındaki artış doğru orantılıdır.
III. Eşit mol sayısında çözünen madde içeren çözeltilerde çözücü miktarı arttıkça, çözeltinin kaynamaya başlama sıcaklığındaki artış azalır.
sonuçlarından hangilerine ulaşabilir?
Yalnız I. | |
I ve II. | |
I ve III. | |
II ve III. | |
I, II ve III. |
Soru 10 |

Görsellerdeki işlemler aşağıdaki ifadelerden hangisine örnek gösterilebilir?
Su içinde uçucu madde çözünürse suyun buhar basıncı yükselir. | |
Dış atmosfer basıncı artınca suyun kaynama noktası artar. | |
Çözünen katı miktarı arttıkça çözeltinin buhar basıncı düşer. | |
Suda çözünen maddeler suyun donma noktasını düşürür. | |
Maddenin saflık oranı arttıkça hâl değişim sıcaklığı artar. |
11. Sınıf Kimya Tarama Testi PDF Test
11. Sınıf Kimya Tarama Testi konusuyla ilgili sorular bulunmaktadır. Testler; kazanım odaklı güncel sorulardan oluşmaktadır.
Test İstatistikleri (Ortalama)
Başarı Tablosu
| İsim Soyisim | Doğru | Yanlış | Süre |